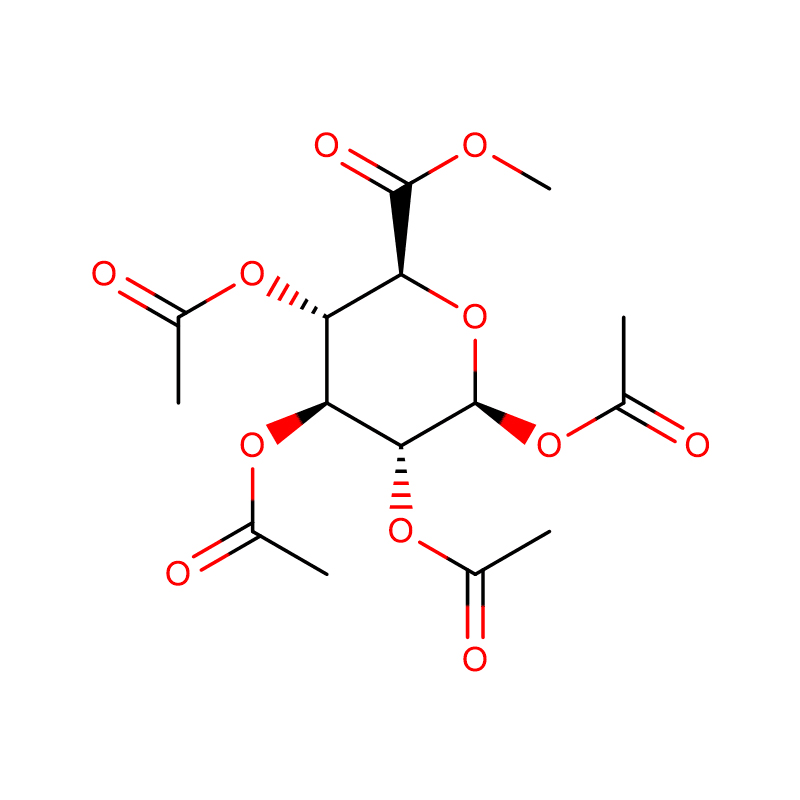
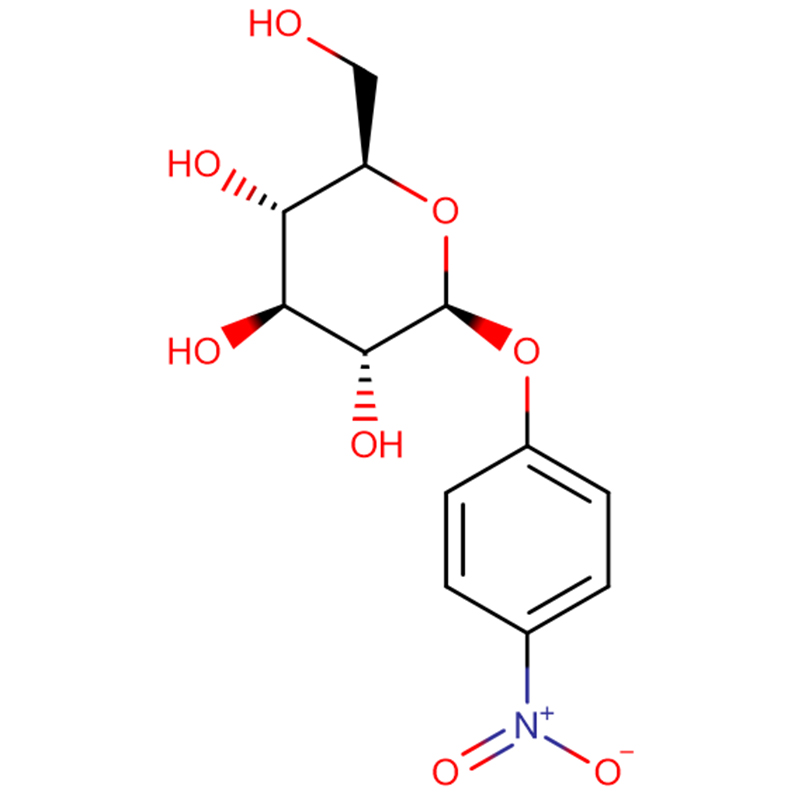
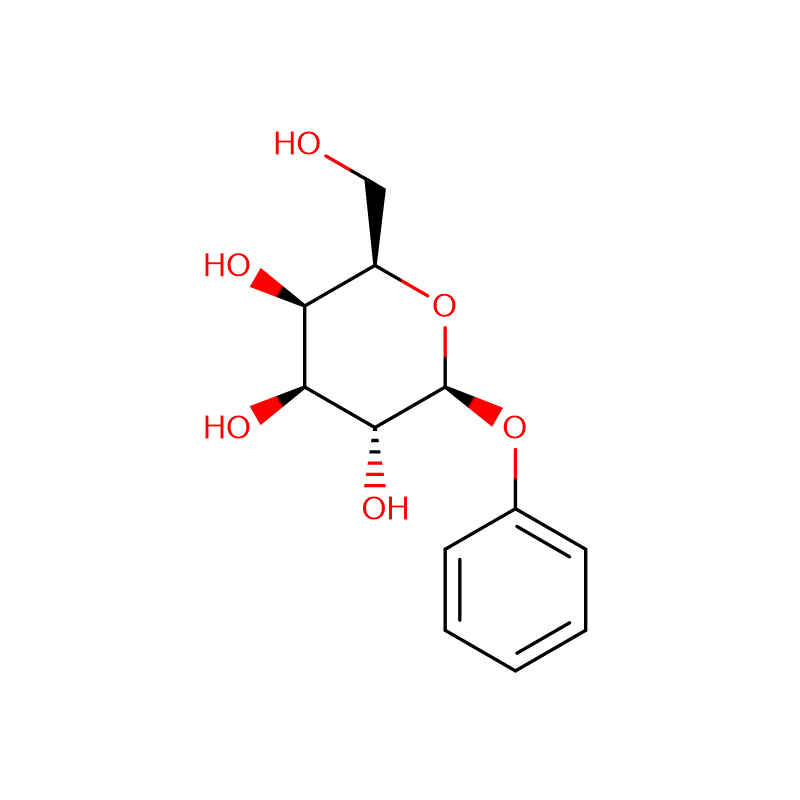
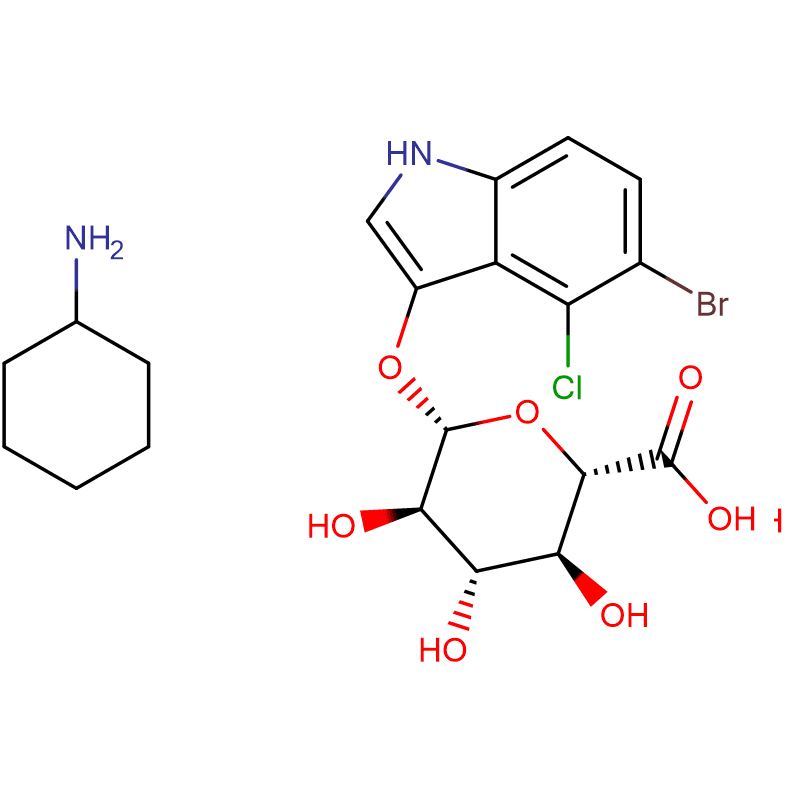
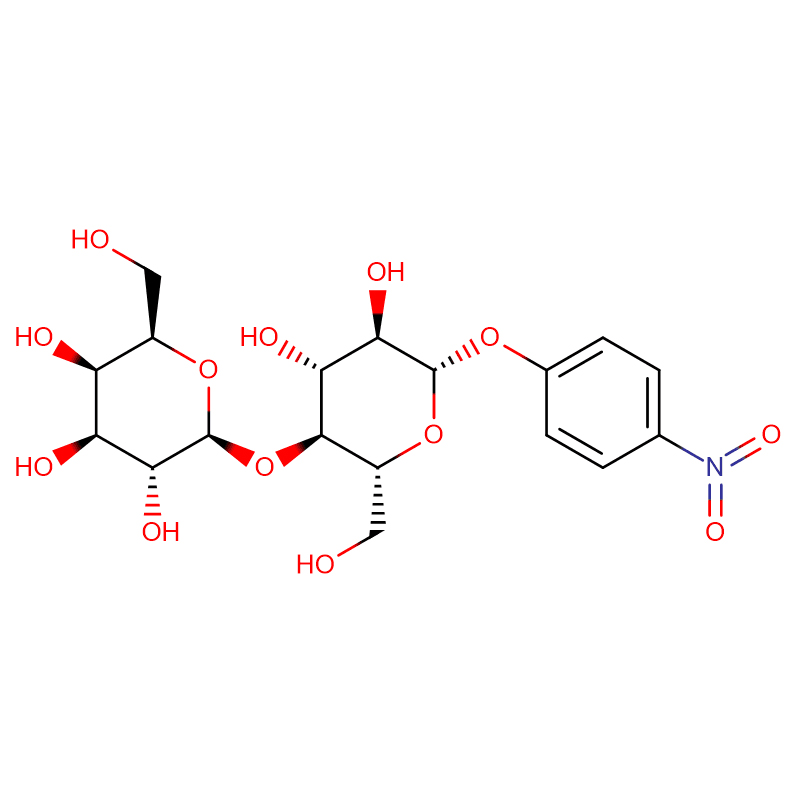
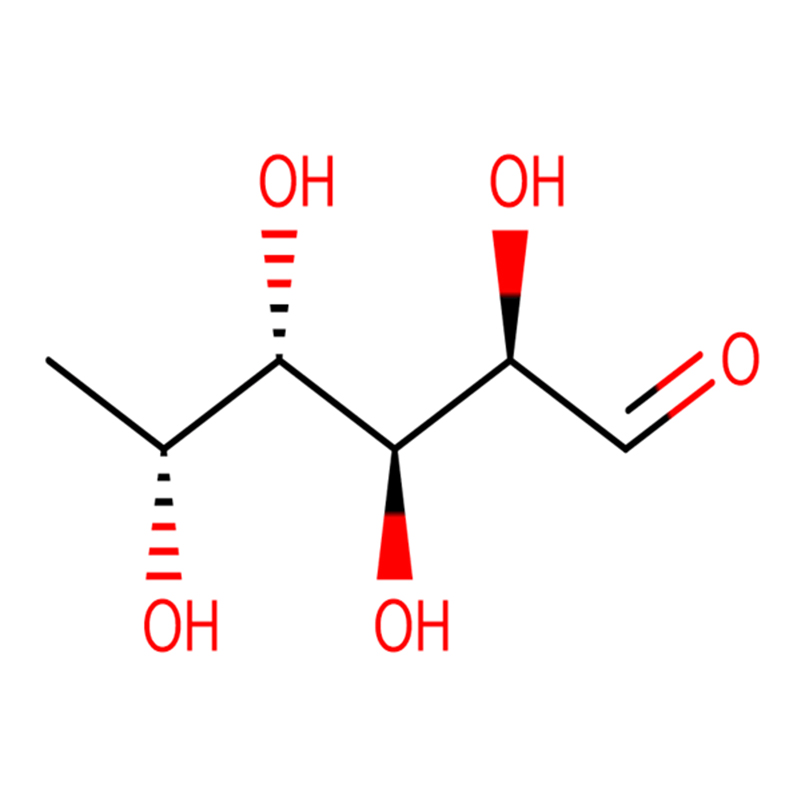
Два ізомерних біцикло[4.1.0]гептанових аналогів інгібітора глікозидази галактовалідаміну, (1R*,2S,3S,4S,5S,6S*)-5-аміно-1-(гідроксиметил)біцикло[4.1.0]гептан -2,3,4-тріол, були синтезовані в 13 етапів з 2,3,4,6-тетра-O-бензил-D-галактози.Інгібіторну активність двох конформаційно обмежених амінів та їхніх відповідних ацетамідів вимірювали проти комерційних ферментів альфа-галактозидази з кавових зерен та E. coli.Активність ферменту GH27 сімейства глікозилгідролаз (кавове зерно) конкурентно інгібується 1R,6S-аміном (7), взаємодія зв’язування, яка характеризується значенням K(i) 0,541 мікромоль.Альфа-галактозидаза E. coli GH36 продемонструвала набагато слабшу взаємодію зв’язування з 1R,6S-аміном (IC(50)= 80 мкМ).Діастереомерний 1S,6R-амін (9) слабо зв’язувався з обома галактозидазами (кавове зерно, IC(50)= 286 мкМ) і (E. coli, IC(50)= 2,46 мМ).